কোভ্যালেন্ট বন্ডস বনাম আয়নিক বন্ডস
কন্টেন্ট
- বিষয়বস্তু: কোভ্যালেন্ট বন্ড এবং আয়নিক বন্ডের মধ্যে পার্থক্য
- তুলনা রেখাচিত্র
- কোভ্যালেন্ট বন্ড কী?
- আয়নিক বন্ড কি?
- মূল পার্থক্য
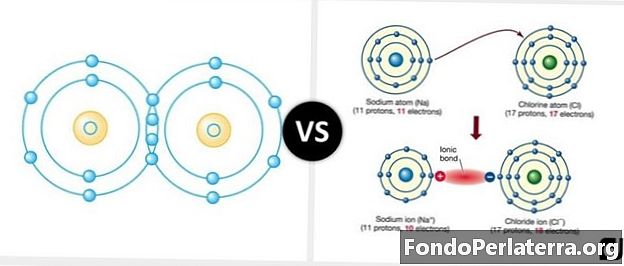
আয়নিক বন্ড এবং সমবায় বাঁধার মধ্যে প্রধান পার্থক্য হ'ল ইলেক্ট্রন জোড়া এবং পরমাণু ভাগ করে নেওয়া। কোভ্যালেন্ট বন্ডে, পারমাণবিকগুলি আয়নিক বন্ধনে থাকার সময় বৈদ্যুতিন-স্তরে একে অপরের দিকে আকৃষ্ট হয়; বৈদ্যুতিন জোড়া পরমাণুর মধ্যে ভাগ করা হয়।
বিষয়বস্তু: কোভ্যালেন্ট বন্ড এবং আয়নিক বন্ডের মধ্যে পার্থক্য
- তুলনা রেখাচিত্র
- কোভ্যালেন্ট বন্ড কী?
- আয়নিক বন্ড কি?
- মূল পার্থক্য
- ভিডিও ব্যাখ্যা
তুলনা রেখাচিত্র
| বিভেদ ভিত্তি | সমযোজী বন্ধনের | আয়নিক বন্ড |
| সংজ্ঞা | কোভ্যালেন্ট বন্ড হ'ল এক ধরণের রাসায়নিক বন্ধন যা পারমাণবরের মধ্যে ভাগ করে নেওয়া বা বন্ডিং জোড় (ইলেকট্রন জোড়া) ভাগ করে জড়িত। | আয়নিক বন্ড হ'ল রাসায়নিক বন্ধনের প্রকার যা একটি পরমাণুর দ্বারা এক বা একাধিক ইলেকট্রনকে ভাগ করে নেওয়া বা মোট পরমাণুকে জড়িত করে। |
| ঘটা | কোভ্যালেন্ট বন্ডগুলি নিরপেক্ষ পরমাণুর মিথস্ক্রিয়ার ফলাফল of | আয়নিক বন্ডগুলি অ্যানিয়নস এবং কেশনগুলির মধ্যে মিথস্ক্রিয়াগুলির ফলাফল। |
| রাসায়নিক সম্ভাবনা | এগুলি বেশ দুর্বল রাসায়নিক বন্ধন | এগুলি হ'ল শক্তিশালী ধরণের রাসায়নিক বন্ধন। |
| গঠন | ধাতববিহীন উপাদানগুলি সমবয়সী বন্ধন গঠন করে | ধাতব উপাদানগুলি আয়নিক বন্ড গঠন করে |
| বৈদ্যুতিন স্থিতি | ভাগ করা ইলেকট্রন | বৈদ্যুতিন মোট স্থানান্তর |
| ম্যাটার রাজ্য | ঘরের তাপমাত্রায় তরল এবং গ্যাস | ঘরের তাপমাত্রায় সলিডস |
| যৌগিক | জৈব | অজৈব |
| দ্রাব্যতা | জলে দ্রবীভূত | জলে দ্রবণীয় |
| আকৃতি | চূড়ান্ত আকার | কোন নির্দিষ্ট আকার |
| নামকরণ | গ্রীক উপসর্গ | রোমান সংখ্যাসমূহ |
| উদাহরণ | হাইড্রো ক্লোরিক অ্যাসিড এবং মিথেন | সালফিউরিক অ্যাসিড এবং সোডিয়াম ক্লোরাইড |
কোভ্যালেন্ট বন্ড কী?
কোভ্যালেন্ট বন্ডস, আণবিক বন্ধনের নামেও পরিচিত, রাসায়নিক বন্ধনের প্রকার যা পরমাণুর মধ্যে অংশীদারি জোড় বা বন্ডিং জোড় (ইলেক্ট্রন জোড়া) ভাগ করে জড়িত। বেশিরভাগ অণুতে, ইলেকট্রনগুলি ভাগ করে নেওয়া প্রতিটি পরমাণুকে একটি স্থির বৈদ্যুতিন কনফিগারেশনের সাথে সম্পর্কিত একটি সম্পূর্ণ বাইরের শেলের সমতুল্য পেতে দেয়। যদি বৈদ্যুতিনগুলির সাথে পরমাণুর অনুরূপ সখ্যতা থাকে তবে বৈদ্যুতিনগুলির জন্য একই সখ্যতা এবং পরমাণুর দ্বারা অনুদান দেওয়ার কোনও প্রবণতার কারণে কোভ্যালেন্ট বন্ডগুলি ঘটতে পারে। পরমাণুগুলি অক্টেট কনফিগারেশন পেতে ইলেকট্রনগুলি ভাগ করে এবং আরও স্থিতিশীল এবং শক্তিশালী হয়। সিগমা এবং পাই কক্ষপথের মিথস্ক্রিয়তার কারণে কোভ্যালেন্ট বন্ডগুলি চার প্রকারের বন্ড গঠন করতে পারে যাকে একক, ডাবল, ট্রিপল এবং চতুর্ভুজ বলা যায়। অক্সিজেন পরমাণু সর্বোত্তম উদাহরণ যা একটি বদ্ধ শেল গঠনের জন্য দুটি অতিরিক্ত ইলেকট্রন প্রয়োজন হয় যখন হাইড্রোজেন পরমাণুগুলির একটি বন্ধ শেল গঠনের জন্য একটির প্রয়োজন হয়। একটি অক্সিজেন পরমাণু তার দুটি ইলেকট্রন হাইড্রোজেন পরমাণুর সাথে ভাগ করে, তাই উভয়ের পরমাণু বন্ধ শেল বন্ধ করে দেয়। এটি শেষ পর্যন্ত একটি জলের অণু তৈরি করে।
আয়নিক বন্ড কি?
আয়নিক বন্ড হ'ল রাসায়নিক বন্ধনের প্রকার যা একটি পরমাণুর দ্বারা এক বা একাধিক ইলেকট্রনকে ভাগ করে নেওয়া বা মোট পরমাণুকে জড়িত করে। আয়নিক বন্ডগুলি সেই উপাদানগুলির ফল যা সহজেই ইলেক্ট্রন এবং যে উপাদানগুলি ইলেক্ট্রন অর্জন করে তাদের হ্রাস করে। এই ধরনের বন্ডগুলি কুলম্বের আইন হিসাবে বর্ণিত চার্জের মধ্যে মিথস্ক্রিয়তার কারণে অণুগুলিতে মোটেই না। আয়নিক বন্ডগুলি ঘরের তাপমাত্রায় দৃ remain় থাকে কারণ, কয়েক মিলিয়ন আয়ন গঠনের পর্যায়ক্রমিক জালাগুলির সময়, প্রতিটি আয়ন বিপরীত চার্জের বহু আয়ন দ্বারা বেষ্টিত থাকে। নেতিবাচক এবং ধনাত্মক আয়নগুলির মধ্যে ইলেক্ট্রোস্ট্যাটিক আকর্ষণগুলি যৌগকে একসাথে ধারণ করে। আয়নিক বন্ধন প্রক্রিয়া চলাকালীন সামগ্রিক শক্তি স্বাভাবিকভাবে ইতিবাচক যা ইঙ্গিত দেয় যে প্রতিক্রিয়াটি এন্ডোথেরমিক এবং প্রতিকূল। অন্যদিকে, তাদের বৈদ্যুতিন আকর্ষণীয় কারণে এই প্রতিক্রিয়াটি একই সময়ে অনুকূল। আয়নিক বন্ডের একটি সাধারণ উদাহরণ হ'ল সোডিয়াম বা লবণ। সোডিয়াম পরমাণুগুলি দ্রুত ইলেকট্রন দেয় যা ইতিবাচক চার্জের ফলস্বরূপ। ক্লোরিন এই ইলেক্ট্রনগুলি গ্রহণ করে এবং নেতিবাচকভাবে চার্জ করা হয়। এই দুটি বিপরীত চার্জযুক্ত পরমাণু তখন একে অপরকে সোডিয়াম ক্লোরাইড অণু গঠনে আকৃষ্ট করে।
মূল পার্থক্য
- কোভ্যালেন্ট বন্ডে, ইলেক্ট্রন অরবিটালগুলি ওভারল্যাপিং হয় যখন আয়নিক বন্ডগুলির ক্ষেত্রে এগুলি পৃথক।
- আয়নিক বন্ডগুলির তুলনায় শক্ত ও ভঙ্গুর সাথে তুলনামূলকভাবে কোভ্যালেন্ট বন্ডগুলি তুলনামূলকভাবে নরম।
- উভয় ধাতব পরমাণু এবং নন-ধাতব পরমাণু আয়নিক বন্ড গঠনের সাথে জড়িত থাকাকালীন সমবায় বন্ধনের গঠনে; শুধুমাত্র অ ধাতব পরমাণু জড়িত।
- বৈদ্যুতিন ভাগ করার কারণে কোভ্যালেন্ট বন্ডগুলি গঠিত হয় যখন ইলেকট্রন স্থানান্তর করার কারণে আয়নিক বন্ডগুলি গঠন হয়।
- যৌগিক গঠনের সময় অণুগুলি সমবায় বন্ধনে কণা থাকে যখন আয়নিক বন্ডগুলিতে এগুলি ইতিবাচকভাবে চার্জযুক্ত হয় এবং নেতিবাচকভাবে চার্জ আয়ন হয়।
- কোভ্যালেন্ট বন্ডগুলি অ-কন্ডাক্টর এবং অায়োনিক বন্ডগুলি কন্ডাক্টর হয়।
- বৈদ্যুতিনগতিশীলতায় কিছুটা ভিন্ন ভিন্ন পরমাণুর মধ্যে কোভ্যালেন্ট বন্ধন ঘটে। আয়নিক বন্ধন বৈদ্যুতিনগতিশীলতার পার্থক্যের পরমাণুর মধ্যে ঘটে।
- আয়নিক বন্ধনের ক্ষেত্রে আয়নিক বন্ধনের ক্ষেত্রে উচ্চ গলনা এবং একটি ফুটন্ত পয়েন্ট প্রয়োজন। সমবায় বন্ধনের ক্ষেত্রে সমবায় বন্ধনের ক্ষেত্রে কম গলনা এবং ফুটন্ত পয়েন্ট প্রয়োজন।
- মিথেন এবং হাইড্রো ক্লোরিক অ্যাসিড একটি সমবায় সোডিয়াম ক্লোরাইডের সাধারণ উদাহরণ এবং সালফিউরিক অ্যাসিড আয়নিক বন্ধনের উদাহরণ।
- কোভ্যালেন্ট বন্ডগুলির একটি নির্দিষ্ট আকার থাকে যখন আয়নিক বন্ডগুলির কোনও নির্দিষ্ট থাকে না
- কোভ্যালেন্ট বন্ডে স্বল্পতা থাকে এবং আয়নিক বন্ডগুলিতে উচ্চ মেরুত্ব থাকে।
- 100% কোভ্যালেন্ট অণুগুলি তেলতে দ্রবীভূত হবে, তবে জলে নয় যখন অনেক আয়নিক বন্ডগুলি পানিতে দ্রবীভূত করার ক্ষমতা রাখে তবে তেলে নয়।
- কোভ্যালেন্ট বন্ডগুলি গুরুত্বপূর্ণ কারণ কার্বন অণুগুলি মূলত কোভ্যালেন্ট বন্ধনের মাধ্যমে ইন্টারঅ্যাক্ট করে এবং আয়নিক বন্ডগুলি গুরুত্বপূর্ণ কারণ এগুলি নির্দিষ্ট জৈব যৌগগুলির সংশ্লেষণের অনুমতি দেয়।
- কোভ্যালেন্ট বন্ড দুটি উপাদান এবং যৌগিক হতে পারে যখন আয়নিক বন্ডগুলি কেবল যৌগিক হতে পারে।