ইস্টার বনাম ইথার

কন্টেন্ট
ইস্টার এবং ইথার হ'ল অক্সিজেন পরমাণুগুলির সাথে জৈব অণু। উভয়ের ইথার সংযোগ রয়েছে যা –O-। এস্টারদের গোষ্ঠীটি রয়েছে - কোও। একটি অক্সিজেন পরমাণু কার্বনে ডাবল বন্ডের সাথে আবদ্ধ হয় এবং অন্য অক্সিজেন একটি একক বন্ধনের সাথে আবদ্ধ হয়। যেহেতু কেবল তিনটি পরমাণু কার্বন পরমাণুর সাথে সংযুক্ত, তাই এটির চারপাশে এটি একটি ত্রিভুজ প্লানার জ্যামিতি রয়েছে। আরও, কার্বন পরমাণু এসপি হয়2hybridized।
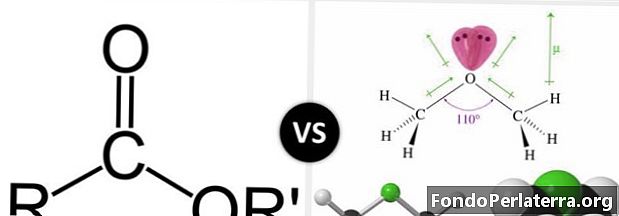
কারবক্সিল গ্রুপটি রসায়ন এবং জৈব রসায়নের একটি বিস্তৃত ক্রিয়ামূলক গ্রুপ। এই গোষ্ঠীটি এসাইল যৌগিক হিসাবে পরিচিত যৌগগুলির সম্পর্কিত পরিবারের পিতামাতা। অ্যাকিল যৌগগুলি কার্বোঅক্সিলিক অ্যাসিড ডেরাইভেটিভস হিসাবেও পরিচিত। এসটার এর মতো একটি কার্বোঅক্সিলিক অ্যাসিড ডেরাইভেটিভ। যৌগিক এস্টারটির সাথে একটি কার্বন-কার্বনিল-অক্সিজেন বন্ধন রয়েছে, অন্যদিকে ইথার যৌগটিতে কার্বন-অক্সিজেন-কার্বন বন্ধন রয়েছে।
সূচিপত্র: ইস্টার এবং ইথারের মধ্যে পার্থক্য
- ইস্টার কী?
- ইথার কী?
- মূল পার্থক্য
- ভিডিও ব্যাখ্যা
ইস্টার কী?
এস্টারদের কাছে আরসিওওআর’র একটি সাধারণ সূত্র রয়েছে। অ্যালকোহল সহ কার্বক্সিলিক অ্যাসিডের মধ্যে প্রতিক্রিয়া দ্বারা এস্টারগুলি তৈরি করা হয়। প্রথমে অ্যালকোহল থেকে প্রাপ্ত অংশের নাম লিখে এস্টারগুলির নামকরণ করা হয়। তারপরে অ্যাসিড অংশ থেকে প্রাপ্ত নামটি শেষের সাথে লেখা হয় -ate বা -oate.

ইথার কী?
ইথারদের কার্যকরী গোষ্ঠী ROR যেমন। Ethoxypropane। ইথার এমন একটি যৌগ যা কার্বন অক্সিজেন-কার্বন বন্ধন ধারণ করে। ইথারগুলি অ্যালকোহলগুলির আন্তঃব্লিকুলার ডিহাইড্রেশন দ্বারা উত্পাদিত হতে পারে। এটি সাধারণত অ্যালকিনের ডিহাইড্রেশনের চেয়ে কম তাপমাত্রায় হয়।

মূল পার্থক্য
- এস্টারগুলি কার্বোক্সেলিক অ্যাসিড ডেরাইভেটিভস এবং গ্রুপ-কোও গ্রুপ রয়েছে। ইথারদের কার্যকরী গোষ্ঠী রয়েছে।
- Terও-অক্সিজেন সংলগ্ন এস্টারের একটি কার্বনিল গ্রুপ রয়েছে, তবে ইথারের তেমন কিছু নেই।
- এস্টারগুলির মধ্যে এতগুলি বৈশিষ্ট্যযুক্ত গন্ধ রয়েছে।
- এস্টারগুলির বিপরীতে অ্যালকোহল এবং একটি কার্বোক্সেলিক অ্যাসিড তৈরি করতে এস্টারগুলি সহজেই হাইড্রোলাইজড হয়।
- এস্টারদের ওসগুলির একটিতে সি ডাবল বন্ড এবং অপর ও'র একটি একক বন্ড সহ কার্যকরী গোষ্ঠী আরসিওওআর রয়েছে .g ইথাইল ইথানয়েট। যেখানে ইথারদের কার্যকরী গোষ্ঠী আরওআর রয়েছে .g Ethoxypropane
- ইথার এমন একটি যৌগ যা কার্বন অক্সিজেন-কার্বন বন্ধন ধারণ করে। ইথারের একটি উদাহরণ হল একটি ইথোক্সাইলেট। নীচের যৌগটি লরথ 5 5. অন্যদিকে, একটি এস্টার একটি যৌগ যা কার্বন-কার্বনিল-অক্সিজেন কার্বন বন্ধন রয়েছে has
- প্রাথমিক বৈশিষ্ট্য যা ইস্টার থেকে ইস্টারকে পৃথক করে তাদের হ'ল পৃথক কাঠামো। ইস্টার হিসাবে পরিচিত যৌগটিতে একটি কার্বন-কার্বনিল-অক্সিজেন বন্ধন রয়েছে, অন্যদিকে ইথার যৌগটিতে কার্বন-অক্সিজেন-কার্বন বন্ধন রয়েছে।
- এস্টারগুলি পোলার যৌগিক, তবে অক্সিজেনের সাথে হাইড্রোজেন-বন্ডেড না থাকার কারণে একে অপরের কাছে শক্তিশালী হাইড্রোজেন বন্ধন তৈরি করার ক্ষমতা তাদের নেই। ফলস্বরূপ, অ্যাসিড বা অ্যালকোহলগুলির সাথে অনুরূপ আণবিক ওজনের তুলনায় এস্টারগুলির কম ফুটন্ত পয়েন্ট থাকে have ইথারগুলি অ্যালকোহলগুলির আন্তঃব্লিকুলার ডিহাইড্রেশন দ্বারা উত্পাদিত হতে পারে। এটি সাধারণত অ্যালকিনের ডিহাইড্রেশনের চেয়ে কম তাপমাত্রায় হয়। উইলিয়ামসন সংশ্লেষণ অপ্রত্যাশিত ইথার উত্পাদন করার অন্য পদ্ধতি।





